山本(玲)グループ
造血幹細胞・加齢・血液疾患

研究概要
“幹細胞” は自己複製能と多分化能を有する特異的な細胞で、全身の細胞の恒常性を維持していますが、加齢とともに機能が変化してその恒常性が破綻し、様々な疾患の原因となることが知られています。私たちのグループは、幹細胞の中でも特に、臨床応用されている血液の幹細胞(造血幹細胞)に着目して研究を行っています。
造血幹細胞は、シングルセル移植でも全身の血液系を再構成できる細胞ですが、加齢によりある特定の造血幹細胞が増加し(クローナル造血)、これが血液疾患などに関与することが知られています。しかし、そのメカニズムは明らかになっていません。
そこで私たちは、マウス・非ヒト霊長類・ヒトをモデルとして用い、様々な最先端計測技術を組み合わせ、 (1) 造血幹細胞の自己複製・多分化能のメカニズム、(2) 加齢に伴う造血幹細胞の機能低下、クローナル造血のメカニズム、(3)急性白血病・骨髄異形成症候群・リンパ腫などの血液疾患の病態を解明することを目指します。こうした理解を通じて、再生医療の進歩につながる幹細胞の維持・増幅技術の開発や、各種の病態の理解・解明、治療法の開発を目指しています。
そのために、以下のようなプロジェクトを行っています。
- 造血幹細胞を対象とした各種シングルセル解析(シングルセル移植、シングルセルRNAシークエンス、シングルセルATACシークエンスなど)を行い、造血幹細胞のバイオロジー・分子機序を解明する。
- 遺伝子改変モデル動物を作出(マウス・非ヒト霊長類)し、加齢・血液疾患の分子機序を解明する。
- 上記の解析に数学など他分野の解析技術を組み合わせ、新しいバイオロジーを創生する。
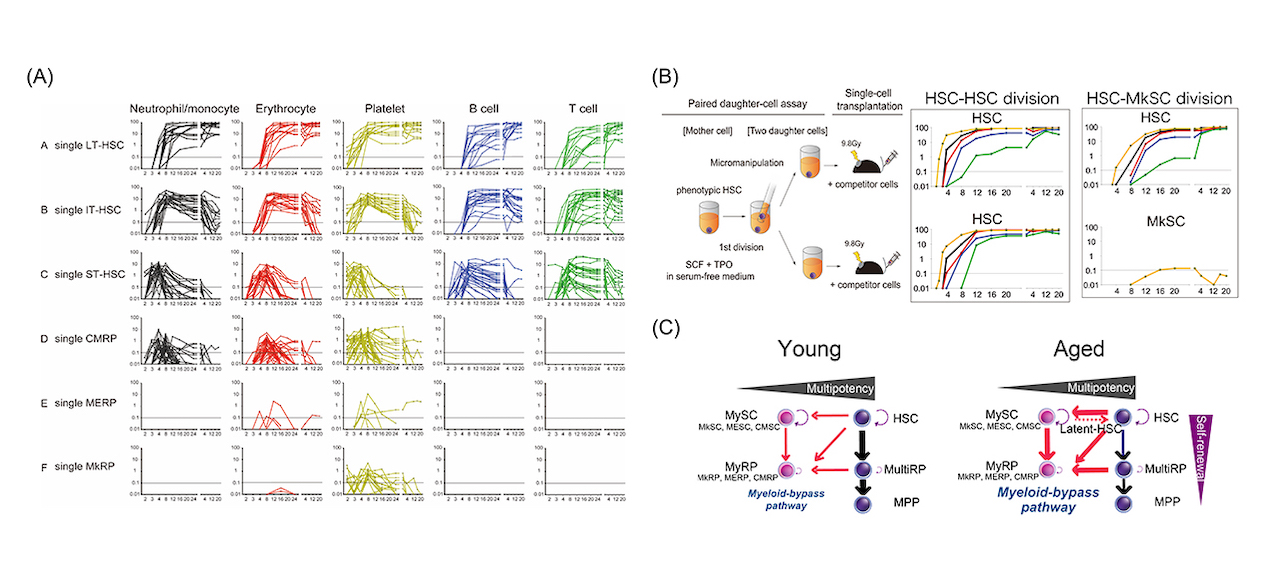
図1. (A) 造血幹細胞のシングルセル移植による末梢血5系統(赤血球・好中球・Bリンパ球・Tリンパ球・血小板)のキメリズム動態。(B) Paired-daughter cell assay によりシングル造血幹細胞の分裂パターンをシングルセル移植により観察。造血幹細胞-造血幹細胞の分裂パターン、造血幹細胞と血小板のみを産生する”造血幹細胞”の分裂パターンを同定。(C)新しい血液分化モデル myeloid-bypass pathwayの提唱とその加齢による変化。
図2. 研究の概略
メンバー

山本 玲
- Position
- 特定拠点准教授
- Laboratory Website
-
https://ashbi.kyoto-u.ac.jp/lab-sites/ryo-yamamoto/
-
大江原 淳
特定職員
-
佐藤 登志⼦
研究員(非常勤)
-
吉岡 真智子
技術補佐員
-
寳生 夏稀
派遣職員
-
今村 啓明
大学院生
-
鈴木 優太
大学院生
-
賓 怜恩(Youngeun Been)
大学院生
論文
Wilkinson, A. C.*, R. Ishida*, M. Kikuchi, K. Sudo, M. Morita, R. V. Crisostomo, R. Yamamoto, K. M. Loh, Y. Nakamura, M. Watanabe, H. Nakauchi, and S. Yamazaki. “Long-term ex vivo expansion of hematopoietic stem cells affords non-conditioned transplantation.” Nature, 571(2019): 117-121. (*Equal contribution)
Yamamoto, R.*, A. C. Wilkinson*, and H. Nakauchi. “Changing concepts in hematopoietic stem cells.”Science, 362 (2018): 895-96.(*Equal contribution)
Yamamoto, R., A. C. Wilkinson, J. Ooehara, X. Lan, C. Y. Lai, Y. Nakauchi, J. K. Pritchard, and H. Nakauchi. “Large-Scale Clonal Analysis Resolves Aging of the Mouse Hematopoietic Stem Cell Compartment.” Cell Stem Cell, 22 (2018): 600-07 e4.
Ghosn, E. E., J. Waters, M. Phillips, R. Yamamoto, B. R. Long, Y. Yang, R. Gerstein, C. A. Stoddart, H. Nakauchi, and L. A. Herzenberg. “Fetal Hematopoietic Stem Cell Transplantation Fails to Fully Regenerate the B-Lymphocyte Compartment.” Stem Cell Reports, 6 (2016): 137-49.
Matsunawa, M.*, R. Yamamoto*, M. Sanada*, A. Sato-Otsubo, Y. Shiozawa, K. Yoshida, M. Otsu, Y. Shiraishi, S. Miyano, K. Isono, H. Koseki, H. Nakauchi, and S. Ogawa. “Haploinsufficiency of Sf3b1 Leads to Compromised Stem Cell Function but Not to Myelodysplasia.” Leukemia, 28 (2014): 1844-50.(*Equal contribution)
Yamamoto, R.*, Y. Morita*, J. Ooehara, S. Hamanaka, M. Onodera, K. L. Rudolph, H. Ema, and H. Nakauchi. “Clonal Analysis Unveils Self-Renewing Lineage-Restricted Progenitors Generated Directly from Hematopoietic Stem Cells.” Cell, 154 (2013): 1112-26.(*Equal contribution)
Ghosn, E. E., R. Yamamoto, S. Hamanaka, Y. Yang, L. A. Herzenberg, H. Nakauchi, and L. A. Herzenberg. “Distinct B-Cell Lineage Commitment Distinguishes Adult Bone Marrow Hematopoietic Stem Cells.” Proc Natl Acad Sci USA, 109 (2012): 5394-8.
Yoshida, K*., M. Sanada*, Y. Shiraishi*, D. Nowak*, Y. Nagata*, R. Yamamoto, Y. Sato, A. Sato-Otsubo, A. Kon, M. Nagasaki, G. Chalkidis, Y. Suzuki, M. Shiosaka, R. Kawahata, T. Yamaguchi, M. Otsu, N. Obara, M. Sakata-Yanagimoto, K. Ishiyama, H. Mori, F. Nolte, W. K. Hofmann, S. Miyawaki, S. Sugano, C. Haferlach, H. P. Koeffler, L. Y. Shih, T. Haferlach, S. Chiba, H. Nakauchi, S. Miyano, and S. Ogawa. “Frequent Pathway Mutations of Splicing Machinery in Myelodysplasia.” Nature, 478 (2011): 64-9.(*Equal contribution)
Yamamoto, R., M. Nishikori, M. Tashima, T. Sakai, T. Ichinohe, A. Takaori-Kondo, K. Ohmori, and T. Uchiyama. “B7-H1 Expression Is Regulated by Mek/Erk Signaling Pathway in Anaplastic Large Cell Lymphoma and Hodgkin Lymphoma.” Cancer Sci, 100 (2009): 2093-100.
Yamamoto, R., M. Nishikori, T. Kitawaki, T. Sakai, M. Hishizawa, M. Tashima, T. Kondo, K. Ohmori, M. Kurata, T. Hayashi, and T. Uchiyama. “PD-1-PD-1 Ligand Interaction Contributes to Immunosuppressive Microenvironment of Hodgkin Lymphoma.” Blood, 111 (2008): 3220-4.
