ニュース
2023.12.6
ナイーブ型ヒト多能性幹細胞による非統合胚モデルを用いて 着床前から原腸陥入初期までのヒト初期発生を再現
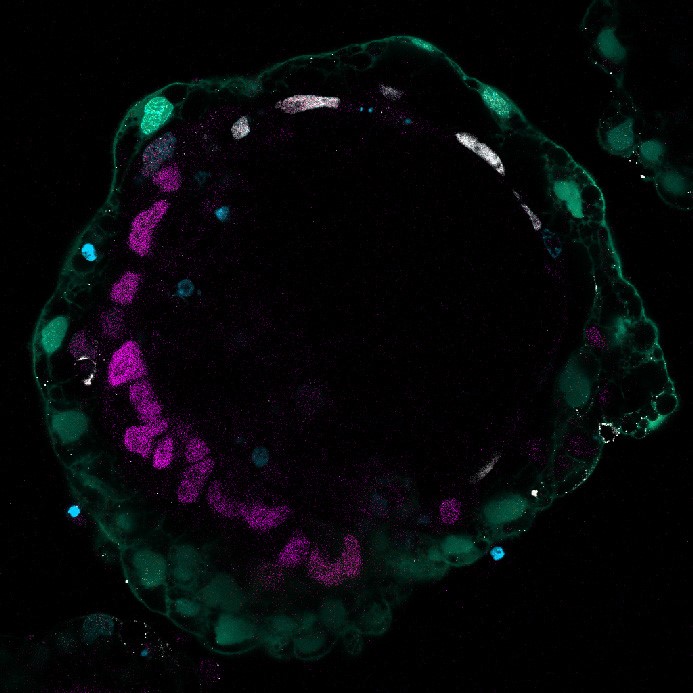
バイラミノイド:
GFP(緑:GATA6誘導型ナイーブ型多能性幹細胞由来原始内胚葉様細胞)、OCT3/4(赤:未分化マーカー)、GATA3(白:羊膜上皮細胞マーカー)DAPI(青:細胞核)
- ナイーブ型 注1 ヒト多能性幹細胞を用いて、着床前の原始内胚葉 注2 へ誘導する方法を開発した。
- 着床前の原始内胚葉およびエピブラスト 注3 の2種の細胞をナイーブ型ヒト多能性幹細胞から同時に誘導することで、二層性胚盤 注4 に類似の構造(バイラミノイド)を形成した。
- バイラミノイドを形成する2種の細胞と栄養膜細胞 注5 が相互作用する非統合胚モデル 注6 を作製し、前後軸の形成や着床後にみられる特定の細胞群への分化などを再現した。
- 非統合胚モデルを用いて、胚体外組織を形成する原始内胚葉や栄養膜細胞がヒト胚の着床期の発生を進めるメカニズムの一端を解明した。
大久保巧研究員(CiRA未来生命科学開拓部門)、山本 拓也 准教授(CiRA同部門、京都大学高等研究院ヒト生物学高等研究拠点WPI-ASHBi)、髙島康弘准教授(CiRA同部門)らの研究グループは、着床前の胚である胚盤胞 注7 を構成する3種の細胞をナイーブ型ヒト多能性幹細胞(iPS細胞とES細胞)から誘導し共培養することで、三次元発生モデルの構築を行いました。
本研究では、着床前という早期の発生段階に類似の3系統の細胞による二層性胚盤および非統合胚モデルを用いて、着床前から、胚の形態や体細胞分化などの大きな変化がみられる原腸陥入初期までの発生を再現しました。また、胚体外組織を形成する原始内胚葉と栄養外胚葉の着床前後の役割を解析することで、本モデルが着床前後のヒト胚発生を詳細に理解するための有用なツールとなることを示しました。
今後は本成果を発展させ、これまでヒトの胚では解析が難しかったヒト発生の詳細な理解を深めるとともに、より自然な発生過程を再現することでヒト多能性幹細胞から組織や臓器を誘導する新たな手法の開発につながることが期待されます。
この研究成果は2023年12月5日(日本時間)に英科学誌「Nature」で公開されました。
詳しい研究成果は こちら用語解説
注1、ナイーブ型:細胞の発生段階や分化多能性の程度を表す用語であり、胚盤胞のエピブラストに相当する状態。
注2、原始内胚葉:胚盤胞を構成する細胞のうち、将来、胚体外組織の一つである卵黄嚢となる細胞。内部細胞塊として、エピブラストと共に胚盤胞に存在し、着床後はエピブラストと二層性胚盤を形成する。
注3、エピブラスト:着床前後の胚に存在する細胞のうち、将来、胎児となり、体を構成する細胞。
注4、二層性胚盤:受精後8日目までに形成されるヒト胚の構造。胚盤胞の内部細胞塊を構成するエピブラストと原始外胚葉の細胞が層状に配列することで形成される。英語ではbilaminar discという。
注5、栄養膜細胞:胚盤胞の外周に存在する栄養外胚葉から分化し、将来、胚体外組織の一つである胎盤を構成する細胞に分化する能力をもつ。
注6、非統合胚モデル:胚の発生を部分的に再現するモデル。胚モデルは、非統合型と胚全体の発生を再現する統合型とに大別される。
注7、胚盤胞:受精後5日目から着床前の胚。エピブラスト、原始内胚葉、栄養外胚葉により構成される。
論文情報
| タイトル | “Hypoblast from human pluripotent stem cells regulates epiblast development” |
| 著者 | Takumi Okubo1, Nicolas Rivron2, Mio Kabata1, Hideki Masaki3,4, Keiko Kishimoto5, Katsunori Semi1, May Nakajima-Koyama1, Haruko Kunitomi1, Belinda Kaswandy1, Hideyuki Sato3,4, Hiromitsu Nakauchi3,4,6, Knut Woltjen1, Mitinori Saitou1,7,8, Erika Sasaki5, Takuya Yamamoto1,7,9,*, Yasuhiro Takashima1,* |
| 掲載誌 | Nature |
| DOI | 10.1038/s41586-023-06871-2 |
