ニュース
2020.2.19
生殖細胞が卵母細胞へと分化する仕組みを解明
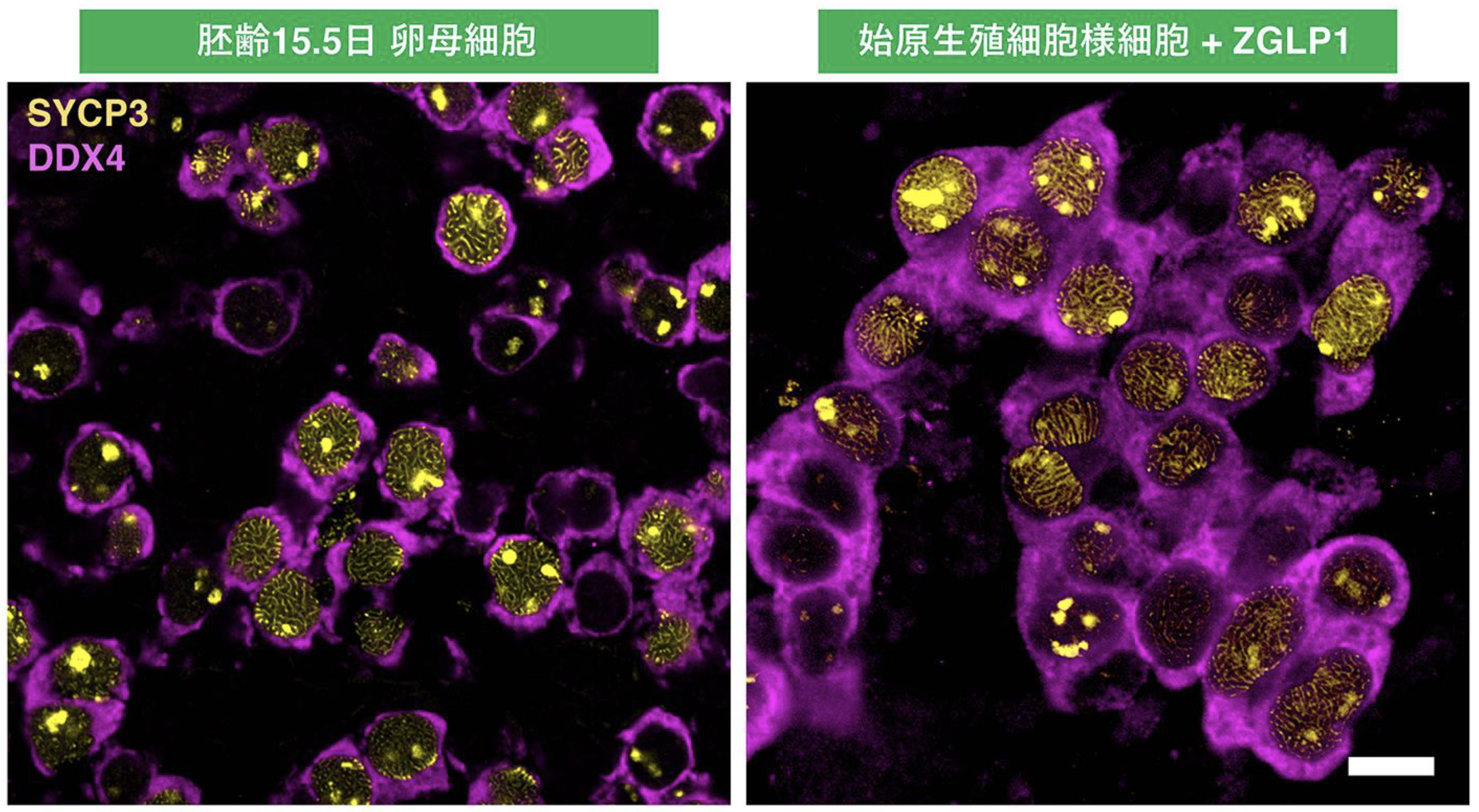
胚齢15.5日目のマウス卵母細胞(左)、転写因子 ZGLP1の効果により卵母細胞へと分化した始原生殖細胞様細胞(右)。減数分裂期に発現するSYCP3(黄色)と生殖細胞特異的に発現するDDX4(マジェンタ)を免疫染色により可視化し分化進行度合いを検証。スケールバー=10μm
概要
京都大学高等研究院ヒト生物学高等研究拠点(ASHBi)拠点長の斎藤通紀教授(兼:京都大学大学院医学研究科教授、京都大学iPS細胞研究所連携主任研究者)、同ASHBiの長岡創特定研究員らは、マウスを用いた実験で、生殖細胞が雌型に性決定し卵母細胞(注1)へと分化する仕組みを世界に先駆けて解明しました。 これまで本研究チームは、マウス多能性幹細胞(注2)からシグナル因子を用いて卵母細胞を誘導することに成功していましたが、その仕組みは不明でした。本研究では、卵母細胞分化の決定因子として、転写因子(注3)Zinc finger GATA like protein 1(ZGLP1)を同定し、その作用機序の詳細な解析を行うことで、どのように雌型の性決定が起こり卵子形成プログラムが開始されるかを明らかにしました。生殖細胞の性決定機構を明らかにした成果であり、将来的にはヒト多能性幹細胞から卵子を誘導する技術開発の促進、不妊症の原因解明などに役立つと期待されます。
本成果は、2020年2月14日(日本時間)に米国科学誌「Science」のオンライン速報版で公開されました。
1.背景
生殖細胞は体の細胞の中で唯一、次世代へとゲノム・エピゲノム(注4)情報を伝えることのできる細胞です。生殖細胞は胎児期の早い段階で他の体細胞とは分けられて発生します。発生直後は生殖細胞の性は決まっておらず(そのような生殖細胞を始原生殖細胞と呼びます)、胎児の成育が進むにつれて雄の個体では精子を作るためのプログラムが活性化され、雌の個体では卵子を作るためのプログラムが活性化されます。これら生殖細胞が性特異的なプログラムを活性化する分子機構は不明でした。近年、生殖細胞の発生過程を理解するための新たなアプローチとして多能性幹細胞から生殖細胞を誘導し、その発生を培養ディッシュ上で再現することにより、生殖細胞の発生・分化の機構を詳細に解析できる実験基盤が開発されました。この実験基盤を活用し、本研究グループはこれまでに骨形成因子(bone morphogenetic protein: BMP)(注5)とビタミンAの代謝産物であるレチノイン酸の二つの液性因子により生殖細胞から卵母細胞への分化が誘導できることを発見していましたが、その作用機序は不明でした。
2.研究方法・成果
本研究は、マウス卵母細胞への分化を誘導する転写因子を同定し、雌型の性決定が行われるための遺伝子発現制御の機序を明らかにすることを目的としました。まず、卵母細胞分化を誘導する候補遺伝子を絞るために、マウス胎児生体内における性決定直後の卵母細胞及び、BMPとレチノイン酸で誘導された培養ディッシュ上の卵母細胞の遺伝子発現情報を用いて八つの候補遺伝子を選出しました。次に、それらの遺伝子を任意のタイミングで発現できるES細胞注1を作製し、始原生殖細胞様細胞(注6)へと分化させた細胞にて候補遺伝子を人工的に発現させ表現型を解析しました。すると胎児期の卵母細胞にて起こる減数分裂(注7)を誘導できることが分かりました。その後、誘導に用いる遺伝子を一つずつ減らしたところ、Zglp1を発現させるベクターを除くと卵母細胞誘導能が極端に落ちること、そしてZglp1を単独で発現させるだけで90%以上の細胞を卵母細胞へと誘導できることが明らかになりました。
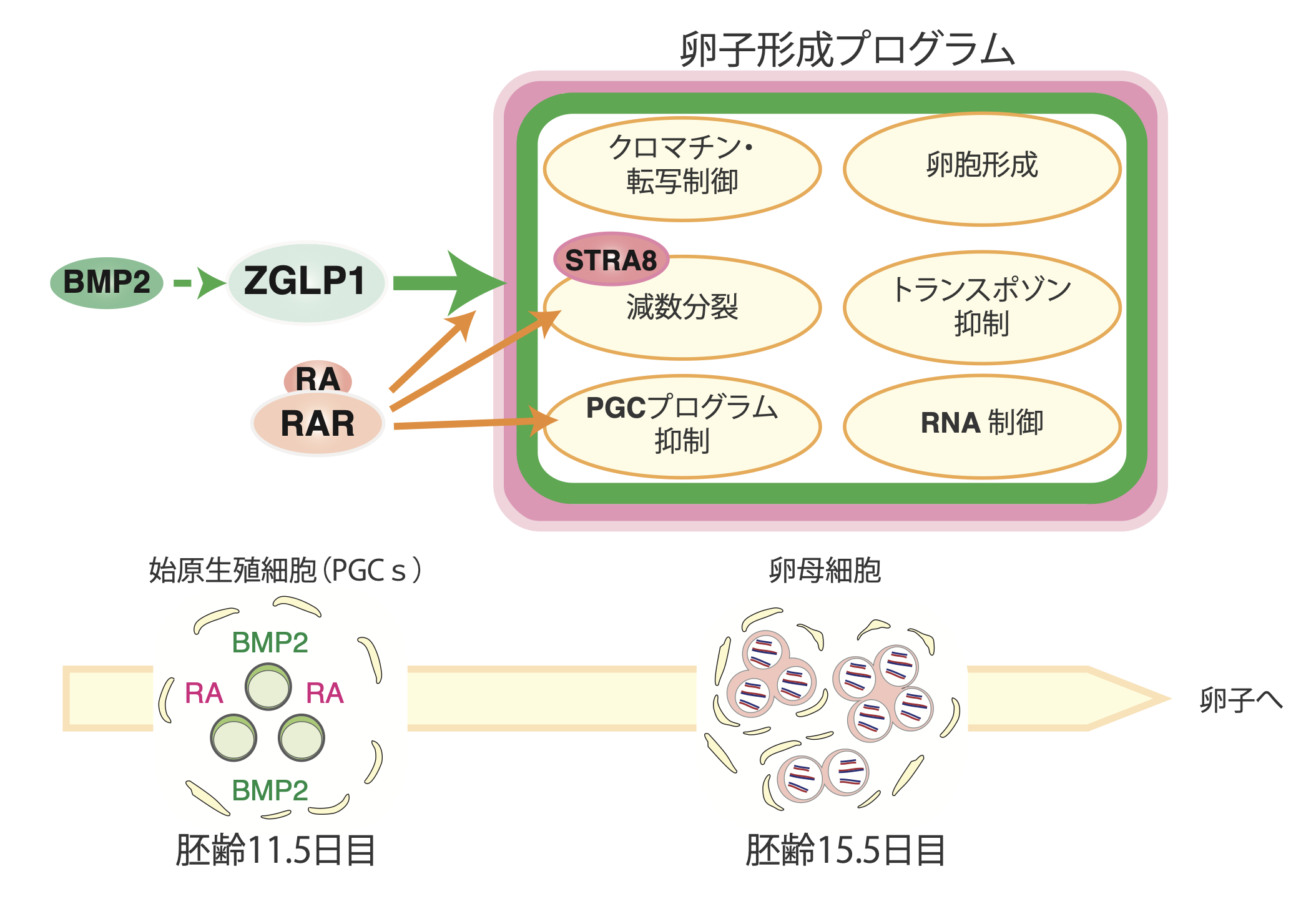
Zglp1の遺伝子欠損マウスを解析したところ、胎児期で減数分裂への移行に支障があり、胚齢17.5日の卵巣では生殖細胞の数が正常マウスの0.6%以下に激減、そして生後8日目までに完全に消失し、その結果、Zglp1遺伝子欠損マウスは不妊に至ることが判明しました。その後、Zglp1とBMP・レチノイン酸シグナルとの関係や、卵母細胞形成に必要と知られている遺伝子群との関係性を網羅的に解析したところ、Zglp1の発現はBMPにより誘起され、BMPの刺激で誘起される卵母細胞形成関連遺伝子の95%以上がZglp1にその発現を依存していることが明らかになりました。そしてBMPとZGLP1が軸となり卵母細胞運命の基盤を構築するのに対し、レチノイン酸シグナル経路は運命決定の促進と補助、そしてPGCプログラムの抑制化という役割を担っていることが明らかになりました。また、ZGLP1は抑制的なエピゲノム状態を有している遺伝子群をより優先的に活性化させることも明らかになりました。
以上より、本研究では今まで不明であった卵形成始動のための遺伝子制御機構が明らかになり、また多能性幹細胞から転写因子のみを用いて卵母細胞を誘導することが可能であることを世界で初めて証明しました。
3.波及効果、今後の予定
本研究では、卵子形成を開始する性分化の仕組みを明らかにしました。今後は機能的な卵子ができるための分子制御機構の更なる解明を目指します。また、精子形成を開始する雄型の性分化の仕組みを明らかにすることを目指します。さらに、ヒト始原生殖細胞様細胞から卵母細胞そして卵子へと分化誘導する方法論の開発を推進します。将来的には不妊症の原因解明、先天性の染色体疾患(注8)の発症機序の解明など、生殖医療の発展に役立つことが期待されます。
4.研究プロジェクトについて
本成果は、以下の事業・研究領域・研究課題によって得られました。
- JST 戦略的創造研究推進事業 総括実施型研究(ERATO)
研究プロジェクト:「斎藤全能性エピゲノムプロジェクト」
研究総括:斎藤 通紀(京都大学 大学院医学研究科 教授)
研究期間:平成23年度~平成28年度 - 日本学術振興会 科学研究費 特別推進研究
「ヒト生殖細胞発生機構の解明とその試験管内再構成」
研究代表者:斎藤 通紀(京都大学 大学院医学研究科 教授)
研究期間:平成29年度~平成33年度 - 日本学術振興会特別研究員
「始原生殖細胞の形成、増殖、分化過程におけるポリコーム因子PRC2の包括的解析」
研究代表者:長岡 創(京都大学ヒト生物学研究拠点特定研究員)
研究期間:平成25年度~平成27年度
用語解説
- 注1 卵母細胞:胎児期に雌型の性決定を受けた始原生殖細胞が分化し、減数分裂注7参照を開始した生殖細胞のこと。卵母細胞が成熟し、減数分裂を完了すると卵子になる。
- 注2 多能性幹細胞:自己複製能力と、身体を構成するほぼ全ての細胞に分化する能力を有する細胞のこと。受精卵から発生する胚盤胞を培養することで樹立される胚性幹細胞(Embryonic Stem Cells: ESCs、ES細胞)や、皮膚などの体細胞に特定の因子(Oct4, Sox2, cMyc, Klf4など)を導入することにより作製される人工多能性幹細胞(induced Pluripotent Stem Cells: iPSCs、iPS細胞)の総称
- 注3 転写因子:DNAに結合して遺伝子の発現を制御し、細胞の機能や運命決定などに影響を与えるタンパク質。
- 注4 エピゲノム:DNAの塩基配列を変えることなく、遺伝子の働きを制御する仕組みをエピジェネティクスと呼び、その情報の集まりをエピゲノムと呼ぶ。ゲノムDNAやDNAが巻き付いているヒストンタンパク質に付与されている様々な化学修飾(メチル化やアセチル化)などを介して作用する。
- 注5 骨形成因子 (bone morphogenetic protein: BMP):細胞から分泌され、他の細胞の運命決定などに影響するタンパク質の一つ。骨の形成を促進する因子として同定されたが、その後、様々な細胞の分化に重要であることが分かった。
- 注6 始原生殖細胞様細胞:始原生殖細胞(Primordial Germ Cells: PGCs)とは、卵子もしくは精子の起源となる細胞。マウスの場合は胚齢6.5日前後に、胚体外胚葉(エピブラスト)内にて一部の細胞が始原生殖細胞として誘導される。始原生殖細胞には雌雄の区別がなく、先行して性決定を受けた生殖巣から生成される因子の影響で、雄では前精原細胞に、雌では卵母細胞に分化する。始原生殖細胞様細胞は、多能性幹細胞から試験管内で誘導した、始原生殖細胞に非常によく似た性質を持つ細胞。マウスの受精後8.5〜9.5日齢の始原生殖細胞に相同であることが、様々な解析から示されている。
- 注7 減数分裂:生殖細胞特異的に起こり、一倍体の配偶子(卵子、精子)を形成する細胞分裂の種類である。減数分裂前期では母方由来、父型由来の1対の相同染色体の間で組換えが起こり、その後、二回の細胞分裂により、まず相同染色体が、次に姉妹染色分体が分離され一倍体の配偶子が形成される。相同染色体間の組換えにより新たな遺伝情報の組み合わせを持つ染色体が形成され遺伝的多様性を創り出す。
- 注8 染色体疾患:ゲノムDNAとタンパク質から構成され遺伝情報の発現と伝達を担うユニットを染色体と呼ぶ。染色体疾患とは染色体の数の変化や形の変化による遺伝情報発現の異常がもたらす疾患である。ヒトでは母体年齢の上昇に伴い卵子の減数分裂期の染色体分離異常の頻度が上がり、ダウン症などの染色体疾患を伴う出生が増えることが知られている。
論文書誌情報
- タイトル
ZGLP1 is a determinant for the oogenic fate in mice(転写因子ZGLP1はマウス生殖細胞の卵子分化への運命を決定付ける) - 著者
長岡 創、中木 文雄、宮内 英孝、野阪 善昭、大田 浩、薮田 幸宏、栗本 一基、林 克彦、中村 友紀、山本 拓也、斎藤 通紀 - 掲載誌
Science - DOI
https://doi.org/10.1126/science.aaw4115
