ニュース
2025.2.14
加齢変化に適応して⼩腸上⽪幹細胞が維持される仕組みを解明
衛生環境の改善や医療の高度化や普及を背景とした高齢化に伴い、国内でも認知症や心血管疾患、がん、糖尿病などの加齢に関連する疾患が増加しており、健康寿命の延伸が喫緊の課題となっています。老化は、加齢に伴う身体の変化であり、生理的な機能の衰えや細胞の性質の変化など生物学的なプロセスの一つとして、分子・細胞・臓器・個体レベルでさまざまな研究が行われています。小腸上皮は、皮膚、筋肉、脳などの臓器・組織と異なり、加齢に伴う変化や疾患が少なく、老化しにくい組織であると一般的に考えられています。しかし、小腸上皮が担っているさまざまな機能をどのように維持し続けているのかは十分にわかっていませんでした。
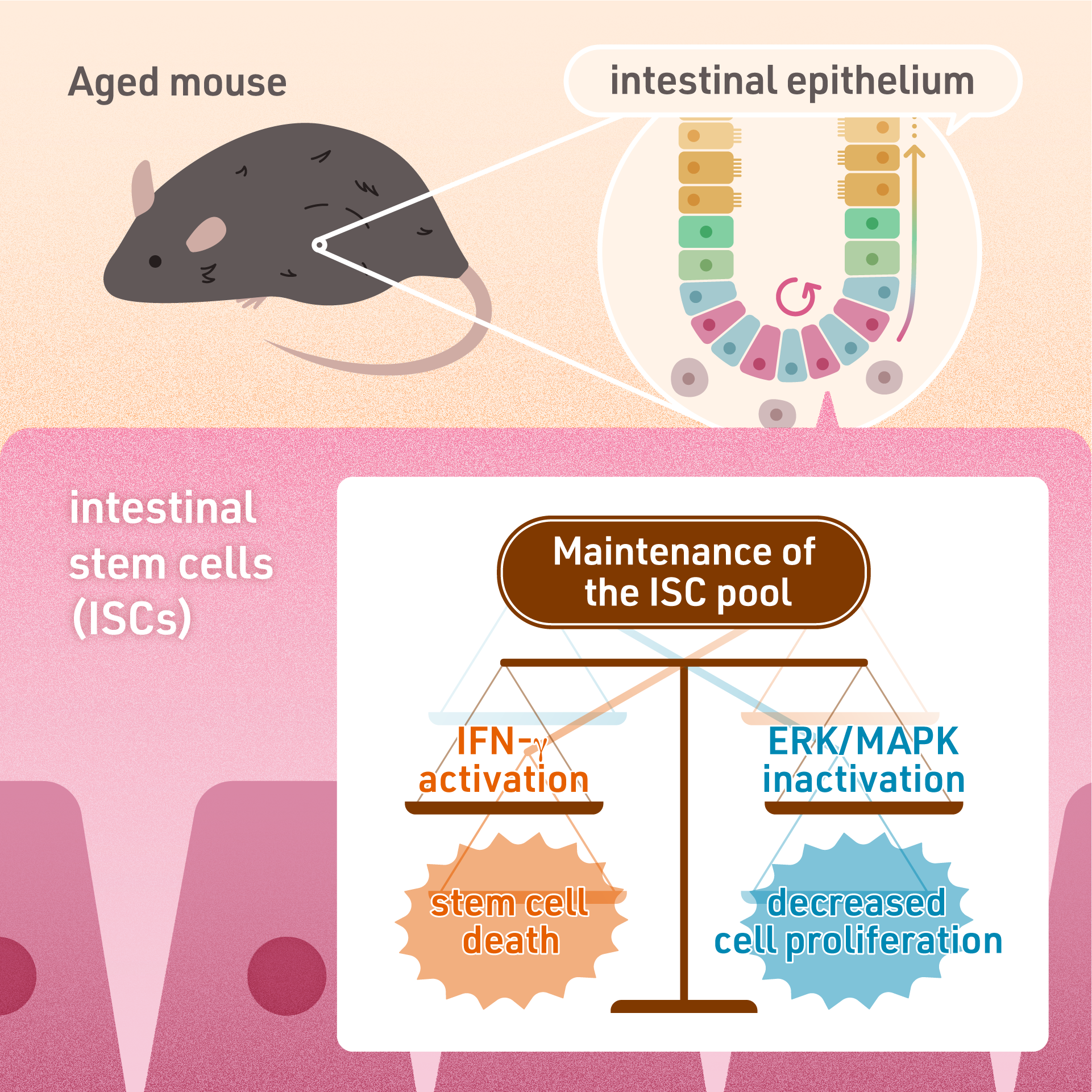
研究概要図
小山明研究員(京都大学iPS細胞研究所(CiRA)未来生命科学開拓部門)、山本拓也准教授(CiRA同部門、京都大学高等研究院ヒト生物学高等研究拠点(WPI-ASHBi))らの研究グループは、小腸上皮を構成する細胞のもととなる小腸上皮幹細胞プールがマウスの生涯にわたって維持される仕組みを明らかにしました。
研究グループは、小腸上皮を構成する細胞の大元となる小腸上皮幹細胞に何らかの抗老化機構が存在するのではないかと考え、マウスの小腸上皮組織を詳細に解析し、加齢に伴って小腸上皮の分化細胞の数や機能が変化する一方で、小腸上皮幹細胞の数や増殖能が維持されていることを見出しました。
さらに、次世代シーケンサーを用いた網羅的な遺伝子発現解析により、小腸上皮幹細胞の遺伝子発現プロファイルが加齢に伴い変化していることなどが明らかになり、その変化を引き起こしていると考えられる小腸上皮幹細胞内のシグナル伝達経路注1を2種類同定しました。マウス生体の解析、さらには小腸オルガノイド培養系を用いた解析を駆使することで、この2種類のシグナル伝達経路の変化が、小腸上皮幹細胞が一生涯にわたって存続するために協調していることを明らかにしました。一方で、この2種類のシグナル伝達経路の変化は分化細胞の加齢変化を誘導することを見出しました。これら分化細胞における加齢変化は、全身性の代謝異常を引き起こす可能性があります。
本研究は、加齢変化に対応した組織幹細胞の維持システムが存在することを初めて明らかにしました。また、小腸上皮幹細胞を長期的に維持する代償として、全身性の加齢性疾患が引き起こされる可能性があることから、このシステムを標的とした個体の健康寿命延伸法の創出につながることが期待されます。
この研究成果は2025年2月13日(米国時間)に国際科学誌「Cell Reports」でオンライン公開されました。
用語解説
注1、 シグナル伝達経路:周囲の環境にあわせて働きを変化させるために、細胞内において⾏われる情報伝達の経路。増殖因⼦やサイトカインなど周囲の環境刺激を受容体が受け取ると、細胞内に情報が伝わり、シグナル伝達経路の活性が切り替えられ、結果として遺伝⼦の発現などが変化する。
書誌情報
Nakajima-Koyama, M., Kabata, M., Lee, J., Sogabe, Y., Sakurai, S., Hirota, A., Kimura, M., Nakamura, T., Imoto, Y., Kometani, K., Hamazaki, Y., Hiraoka, Y., Saitou, M., Nishida, E., & Yamamoto, T. (2025). The balance between IFN-γ and ERK/MAPK signaling activities ensures lifelong maintenance of intestinal stem cells. Cell Reports. https://doi.org/10.1016/j.celrep.2025.115286
