霊長類におけるX染色体遺伝子量補正プログラムを解明
概要
京都大学高等研究院 ヒト生物学高等研究拠点(WPI-ASHBi)拠点長の斎藤通紀 教授(兼:京都大学大学院医学研究科教授、京都大学iPS細胞研究所連携主任研究者)、同ASHBiの岡本郁弘 特定講師らは、カニクイザルを用いた実験で、霊長類におけるX染色体遺伝子量補正プログラムを世界に先駆けて解明しました。
哺乳類の性染色体1構成は、雌はXX、雄はXYです。そのため、雌は雄の2倍量のX連鎖遺伝子2量を持つ事になります。Y染色体の遺伝子は50個ほどなのに対して、X染色体には遺伝子が800個ほどあります。このため、雌雄間でX連鎖遺伝子産物量の差を補正するために、雌では2本のX染色体のうち1本を一括して不活性化するメカニズム「X染色体不活性化3」が存在します。また、2本ある常染色体4との差を補正するためにX連鎖遺伝子の発現量を2倍化する「X連鎖遺伝子のアップレギュレーション5」が存在します。
これらX染色体遺伝子量補正プログラムは胚発生初期に起こるため、ヒトを含む霊長類では、その仕組みについては長らく不明でした。本研究では霊長類のモデル動物であるカニクイザルを用いて、X染色体不活性化に必須のXIST遺伝子6に着目し、胚発生過程におけるその作用機序の詳細な解析を行うことで、霊長類では、いつどのようにX染色体遺伝子量補正が起こるのかを明らかにしました。本成果により、長らく不明であった霊長類の胚発生初期に起こるX染色体遺伝子量補正プログラムの仕組みが明らかになりました。また、本成果はヒト多能性幹細胞7から卵母細胞8を誘導する研究、および着床前後胚培養法の技術開発促進、不妊症の原因解明などに役立つと期待されます。
本成果は、2021年11月19日(日本時間)に米国科学誌「Science」で公開されました。
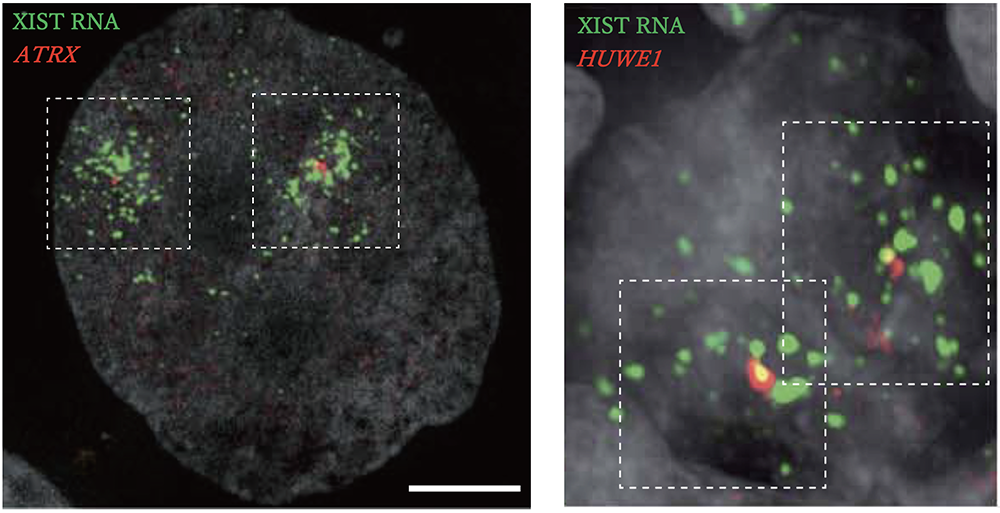
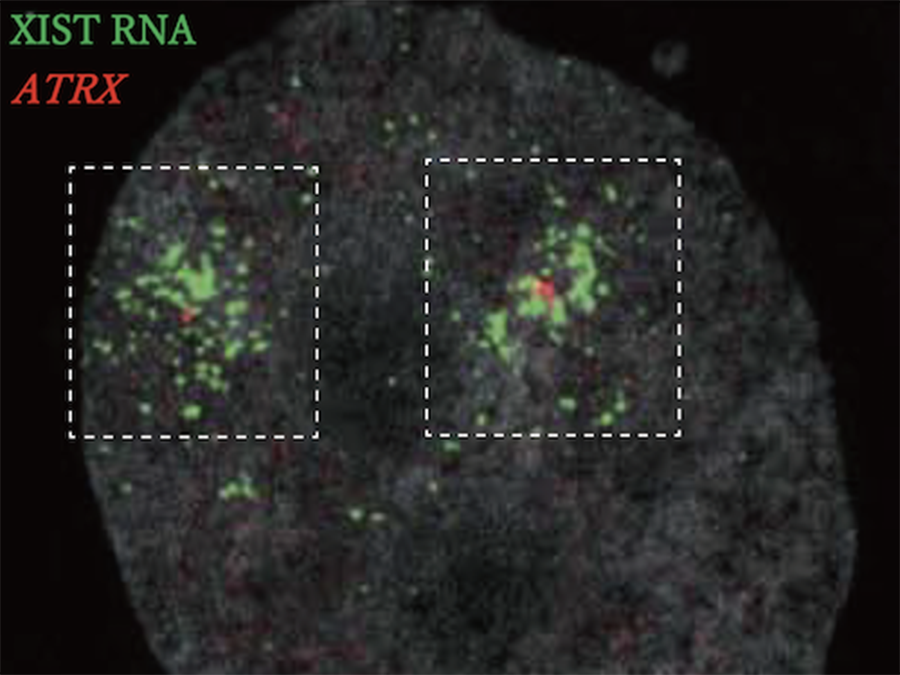
右図:胚齢57日目の始原生殖細胞。XIST RNA(緑)とX連鎖遺伝子(赤)を蛍光 in situ ハイブリダイゼーションにより可視化し不活性化の進行度合いを検証。
1.背景
哺乳類のX染色体遺伝子量補正は胚発生初期の着床前後胚で起こります。マウスでは、X染色体不活性化に必須のXIST遺伝子は2細胞期より、父由来のX染色体からのみ発現し、胚盤胞期に全ての細胞で父由来のX染色体が選択的に不活性化されます。この父由来X染色体の選択的不活性化は着床後、将来、胎盤などを形成する胚体外部では維持されますが、エピブラスト9では再活性化された後、父母由来のX染色体はランダムに不活性化されます。ヒトでは、マウスとは異なり、着床前胚でXIST遺伝子は両方のX染色体から発現しますが、X連鎖遺伝子の発現抑制は起きておらず、いつどのようにX染色体遺伝子量補正が起きるのかは不明でした。
2.研究方法・成果
本研究は、カニクイザルをモデル動物として用いて、霊長類の初期発生過程におけるX染色体遺伝子量補正プログラムを明らかにすることを目的としました。まず、着床前胚におけるXIST とX連鎖遺伝子の発現を解析しました。すると、ヒト着床前胚と同様にXISTは父母由来の両X染色体から発現しているが、X連鎖遺伝子の発現抑制は起こっていないことが分かりました。
次に、早期着床後胚におけるXISTとX連鎖遺伝子の発現を解析したところ、まず、着床後2日目(胚齢11日)にかけて胎盤等になる胚体外部で、次に4(胚齢13日)から6日目(胚齢15日)にかけてエピブラストで、最後に4(胚齢13日)から8日目(胚齢17日)にかけて卵黄嚢でXIST遺伝子の発現が片方のX染色体からのみとなり、X連鎖遺伝子は発現抑制されることが明らかになりました。また、X連鎖遺伝子発現量を解析したところ、着床前から胚齢20日にかけて約2倍まで発現量が上昇し、常染色体とほぼ同レベルに到達していることが明らかになりました。
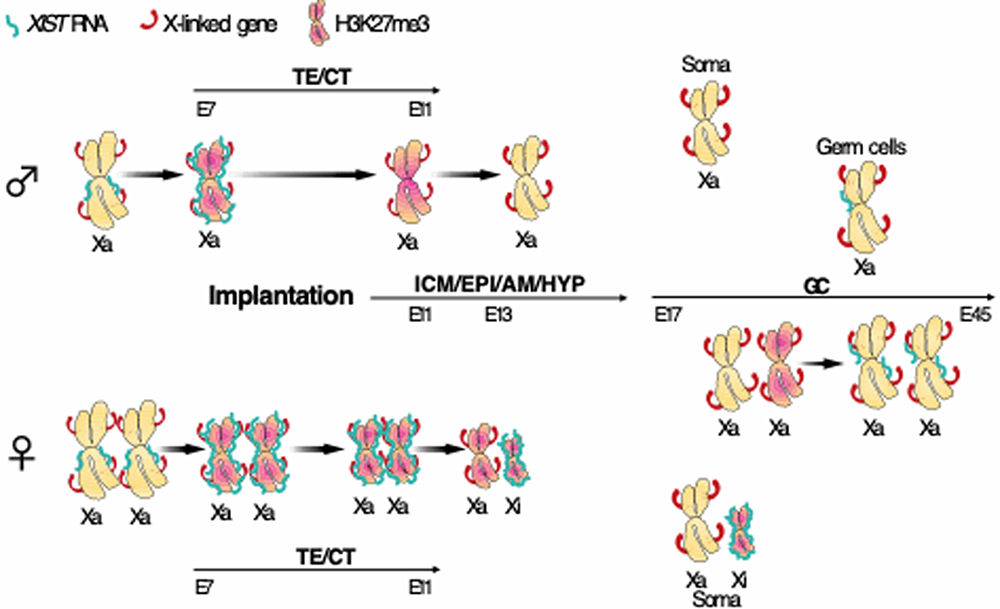
さらに、始原生殖細胞10では分化初期からXIST遺伝子の発現が低下し、両X染色体から遺伝子発現が再開していることが明らかになりました。また、始原生殖細胞が生殖隆起に移動後、両X染色体からXIST遺伝子の発現が再開していることも明らかになりました。
以上より、本研究では今まで不明であった霊長類の初期発生過程と始原生殖細胞の分化過程におけるX染色体遺伝子量補正プログラムを世界で初めて明らかにすることが出来ました。
3.波及効果、今後の予定
本研究では、霊長類におけるX染色体遺伝子量補正プログラムを明らかにしました。今後はさらに霊長類のX染色体遺伝子量補正プログラムの分子制御機構の解明を目指します。また、マウスと同様に培養条件下でX染色体不活性化を再現する方法の開発を推進します。将来的にはヒト多能性幹細胞から卵母細胞を誘導する研究および着床前後胚培養法の技術開発促進、不妊症の原因解明など、生殖医療の発展に役立つことが期待されます。
4.研究プロジェクトについて
本成果は、以下の事業・研究領域・研究課題によって得られました。
- JST 戦略的創造研究推進事業 総括実施型研究(ERATO)
研究プロジェクト:「斎藤全能性エピゲノムプロジェクト」
研究総括:斎藤 通紀(京都大学 大学院医学研究科 教授)
研究期間:平成23年度~平成28年度 - 日本学術振興会 科学研究費 特別推進研究
「ヒト生殖細胞発生機構の解明とその試験管内再構成」
研究代表者:斎藤 通紀(京都大学 大学院医学研究科 教授)
研究期間:平成29年度~平成33年度 - 日本学術振興会 科学研究費 基盤研究 (C)
「霊長類におけるX染色体不活性化機構の解明」
研究代表者:岡本郁弘(京都大学高等研究院ヒト生物学高等研究拠点、ASHBi、特定講師)
研究機関:平成30年度〜平成33年度
用語解説
- 性染色体:雌雄の性決定に関わる遺伝子を持つ雌雄によって形態や数が異なる染色体。 ↩︎
- X連鎖遺伝子:X染色体上にある遺伝子。 ↩︎
- X染色体不活性化:1961年に英国の遺伝学者故Mary F. Lyon博士により発見された生命現象。哺乳類の雌の細胞で2本のX染色体の1本がランダムに、染色体上の遺伝子が一括して転写抑制を受ける現象。 ↩︎
- 常染色体:性染色体以外の雌雄で形態や数に差がない染色体。 ↩︎
- X連鎖遺伝子のアップレギュレーション:1967年に米国の遺伝学者故大野乾博士により発表された仮説。常染色体は雌雄ともに2本あるが、活性X染色体は1本しかないので、常染色体上の遺伝子と発現量を合わせるためにX連鎖遺伝子の転写活性を2倍に亢進していると提唱した。 ↩︎
- XIST (X-inactive specific transcript) 遺伝子:X染色体不活性化の開始に必須の遺伝子。XIST遺伝子から転写されるRNAはタンパク質を構成するアミノ酸配列をコードしないノンコーディングRNA(XIST RNA)。XIST RNA はX染色体上に蓄積してエピジェネティック修飾因子を呼び込み、X染色体のクロマチン注11をヘテロクロマチン注12化すると考えられています。エピジェネティック修飾因子は酵素活性を持ち、クロマチンを構成するヒストン注13に化学修飾を付加して、近傍の標的遺伝子の転写を抑制する。 ↩︎
- 多能性幹細胞:自己複製能力と、身体を構成するほぼ全ての細胞に分化する能力を有する細胞。着床前胚(胚盤胞)の内部細胞塊から樹立した胚性幹細胞 (Embryonic Stem Cells: ESCs, ES細胞、皮膚や血液などの体細胞に特定の因子(OCT4, SOX2, cMYC, KLF4など)を導入することにより作製される人工多能性幹細胞(induced Pluripotent Stem Cells: iPSCs, iPS細胞)の総称。 ↩︎
- 卵母細胞:胎児期に雌型の性決定を受けた始原生殖細胞が分化し、減数分裂を開始した生殖細胞のこと。卵母細胞が成熟し、減数分裂を完了すると卵子になる。 ↩︎
- エピブラスト:多能性細胞からなる細胞集団。 ↩︎
- 始原生殖細胞:始原生殖細胞(Primordial Germ Cells: PGCs)とは、卵子もしくは精子の起源となる細胞。カニクイザルの場合は胚齢11日前後に、羊膜内にて一部の細胞が始原生殖細胞として誘導される。始原生殖細胞には雌雄の区別がなく、先行して性決定を受けた生殖巣から生成される因子の影響で、雄では前精原細胞に、雌では卵母細胞に分化する。 ↩︎
- クロマチン:真核生物において、遺伝情報を担うゲノムDNAとヒストンなどの各種タンパク質との複合体。
- ヘテロクロマチン:クロマチンが凝集した領域。この領域に存在する遺伝子は発現抑制されている。
- ヒストン:真核生物でゲノムDNAと結合して染色体を作るタンパク質群。多種類の化学的修飾を受け、それにより遺伝子の発現が制御される。
論文書誌情報
| タイトル | The X-chromosome dosage compensation program during the development of cynomolgus monkeys |
|---|---|
| 著者 | Ikuhiro Okamoto*, Tomonori Nakamura, Kotaro Sasaki, Yukihiro Yabuta, Chizuru Iwatani, Hideaki Tsuchiya, Shin-ichiro Nakamura, Masatsugu Ema, Takuya Yamamoto, Mitinori Saitou* *Corresponding author |
| 掲載誌 | Science |
| DOI | https://doi.org/10.1126/science.abd8887 |